La résistance des bactéries aux antibiotiques entraîne le décès d’un million de personnes chaque année dans le monde. Mais un vaccin contre le staphylocoque doré suscite l’espoir d’enrayer l’antibiorésistance.
35.000 personnes meurent chaque année d’infections résistantes aux antibiotiques en Europe. Un impact « comparable à celui de la grippe, de la tuberculose et du VIH/SIDA réunis », explique le ministère de la Santé. A l’échelle de la planète, l’antibiorésistance entraîne le décès d’environ 1 million de personnes chaque année, selon l’Organisation mondiale de la santé (OMS).
Un vaccin contre deux souches de staphylocoque doré
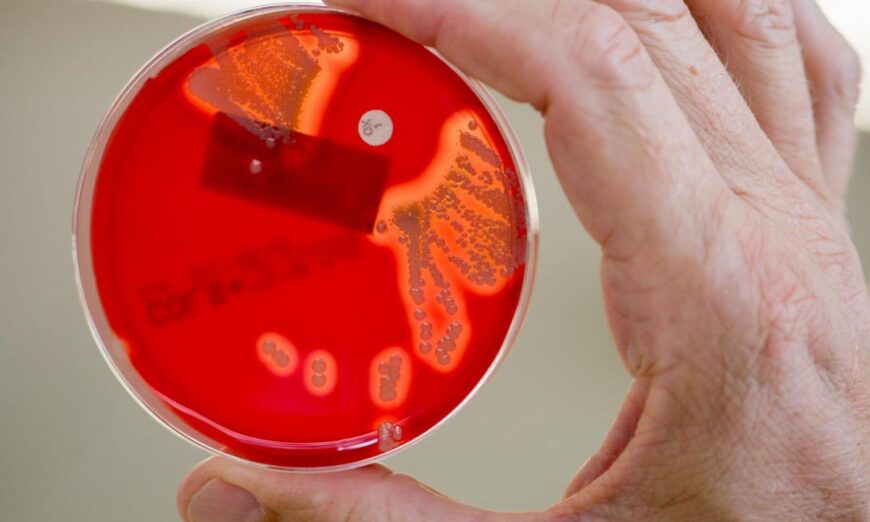
Pour tenter d’enrayer ce fléau, l’une des pistes serait de trouver un vaccin contre les bactéries qui résistent aux antibiotiques. Un espoir dont vient de se rapprocher une équipe de la Michigan State University. Elle vient de mettre au point un vaccin contre le staphylocoque doré et le staphylocoque doré résistant à la méticiline (un antibiotique), deux souches largement responsables d’infections mortelles.
Et son modèle de vaccin, très flexible, pourrait permettre de cibler de nombreuses autres bactéries. Un pas de géant dans la recherche vaccinale publié dans la revue Nature Communications.
Si la découverte des antibiotiques a permis d’améliorer l’espérance de vie, son utilisation a peu à peu installé un problème majeur de santé publique : la résistance aux antibiotiques. A force d’être exposées à cette classe de médicaments, les bactéries développent des mécanismes de défense et mutent. Elles échappent alors à l’action des antibiotiques et continuent de proliférer dans l’organisme. En se multipliant, la bactérie va transmettre sa résistance aux antibiotiques à sa descendance.
Un glucide comme porte d’entrée
Pour couper court à ce cercle vicieux, le vaccin constitue une piste prometteuse. A la base de chaque vaccin, on trouve un antigène, le morceau de virus que l’organisme ou que le vaccin peut identifier afin de l’attaquer. Le corps ou le vaccin l’identifie comme corps étranger et peut créer des anticorps pour combattre l’infection. La plupart des vaccins que nous connaissons utilisent une protéine comme antigène.
On a par exemple beaucoup parlé de la protéine ACE2, « porte d’entrée » des vaccins pour combattre le Covid-19.
Cette fois, l’équipe de la Michigan State University a choisi de se baser sur un glucide. On trouve une couche de glucide à la surface de presque toutes les bactéries. Cette enveloppe collante leur sert à s’attacher aux surfaces autour d’elles. Or, autour du staphylocoque doré, mais aussi chez de nombreuses autres bactéries, se trouve un glucide appelé PNAG. « On sait déjà qu’il joue un rôle crucial dans la virulence de la bactérie.
Sans lui, la survie de la bactérie est largement réduite.
C’est donc plus difficile pour elle de muter. Et c’est donc très difficile d’échapper au système immunitaire », explique à Sciences et Avenir le Pr Xuefei Huang, spécialisé en ingénierie biomédicale et en chimie et qui signe ces travaux.
Les glucides en général, y compris PNAG, sont un peu comme une mosaïque.
Il existe une myriade de façons d’arranger leurs molécules mais seulement quelques-unes d’entre elles auront les effets recherchés par les chercheurs. Modifier rien qu’un élément peut changer la performance de PNAG comme un potentiel antigène. Après avoir créé 32 différentes structures différentes, l’équipe a identifié deux combinaisons particulièrement prometteuses.
Déjà un essai clinique chez l’humain
Maintenant que la porte d’entrée de la bactérie a été identifiée, impossible d’envoyer l’antigène tel quel dans les cellules. Il lui faut, pour arriver à bon port, être transporté par un vaisseau adapté. Pour envoyer PNAG dans l’organisme, l’équipe s’est basée sur une plateforme de bactériophage, un virus capable d’infecter les bactéries.
Appelé Qbeta, il a été modifié afin qu’on puisse le lier avec un glucide et porter un PNAG jusque dans l’organisme. Un choix d’autant plus important que PNAG seul n’est pas capable de provoquer une réponse immunitaire forte. Mais Qbeta, lui, arrive à muscler cette réaction afin que la protection soit plus forte.
Testée chez la souris, la combinaison bactériophage et glucide a montré une protection très élevée contre le staphylocoque doré et le staphylocoque résistant à la méticiline.
Le vaccin est désormais en train d’être testé sur l’Homme dans un essai clinique. Il n’aura pas vocation à annuler l’antibiorésistance chez le patient. Mais plutôt à être administré très en amont dans la vie, afin de tuer les bactéries dangereuses, qu’elles soient déjà résistantes aux antibiotiques ou non.
« Quand les essais cliniques seront terminés, nous proposerons de l’administrer aux enfants pour les protéger d’infections dangereuses, comme on le fait déjà pour la poliomyélite ou les infections à pneumocoques dans les cliniques », détaille le Pr Huang.
Comme le glucide PNAG est retrouvé à la surface de nombreuses bactéries, l’équipe espère faire d’une pierre deux coups.
Ce vaccin pourrait potentiellement être efficace contre de nombreux types de bactéries, pas seulement le staphylocoque doré. Si l’équipe y parvenait, il pourrait donc devenir un vaccin à large spectre, qui cible de multiples pathogènes dangereux pour l’humain.
sciencesetavenir