Des chercheurs américains ont découvert la voie par laquelle les cellules comprennent qu’il est temps de mourir avant de devenir un danger pour le corps.
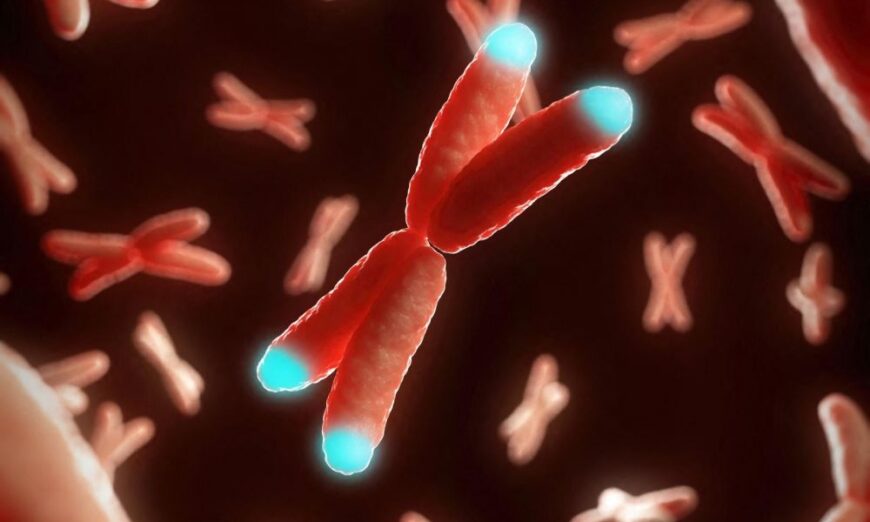
Les cellules ont la sagesse de savoir quand il est temps de passer l’arme à gauche. En vieillissant, des mutations génétiques s’accumulent au sein du génome de nos cellules, augmentant le risque de malfonctionnement… et de cancer. Ce vieillissement est marqué entre autres par un raccourcissement des télomères (les extrémités des chromosomes), qui deviennent de plus en plus court à chaque division cellulaire. Lorsque ces télomères deviennent trop courts, la cellule normalement ne peut plus se multiplier et finit par être détruite par le système immunitaire.
Ce processus assure l’élimination des cellules trop vieilles qui auraient potentiellement accumulé trop de mutations et pourraient donc devenir cancéreuses à cause de ces mutations. Le mécanisme par lequel ce raccourcissement des télomères induisait la destruction de ces cellules était encore méconnu. Mais des chercheurs de l’Institut Salk d’études biologiques en Californie (États-Unis) viennent de dévoiler une partie du système par lequel les cellules lèvent la main pour dire que leur temps est arrivé. Leur étude a été publiée le 8 février 2023 dans la revue Nature.
La barrière ultime pour éviter qu’une cellule devienne cancéreuse
La fonction des télomères est de protéger les extrémités des chromosomes pour que l’ADN ne s’effiloche et pour que les chromosomes ne puissent pas se coller les uns aux autres. À chaque division cellulaire (mitose), les chromosomes sont répliqués pour faire une copie pour chaque cellule résultante. Mais ce mécanisme de réplication ne parvient pas à copier la dernière partie des chromosomes, dans le télomère. Celui-ci devient ainsi de plus en plus court.
À partir d’une certaine longueur, ce raccourcissement active un processus de sénescence ou vieillissement cellulaire, qui notamment empêche ces cellules de continuer à se multiplier. C’est une première barrière contre l’apparition des cellules cancéreuses. Mais certaines cellules échappent à ce mécanisme de contrôle et continuent à se diviser. C’est alors qu’une deuxième barrière est activée, afin de détruire la cellule pour de bon.
Les chercheurs ont observé que les cellules arrivées à ce stade expriment des bouts d’ARN provenant des télomères. Puis, ces morceaux d’ARN activent une molécule immunitaire nommée ZBP1 (pour Z-DNA-binding protein 1 en anglais) qui normalement reconnaît des séquences d’ADN viral lors des infections et active un processus inflammatoire pour défendre la cellule. Lorsque ZBP1 reconnaît ces ARNs des télomères, un processus similaire d’inflammation est activé, entrainant la production d’interférons, des protéines du système immunitaire.
Les télomères communiquent avec les mitochondries pour activer la destruction des cellules trop vieilles
Mais pour être sûr que la menace est prise au sérieux, ZBP1 active une deuxième voie immunitaire. Une fois activées par l’ARN des télomères, plusieurs molécules de ZBP1 se collent ensemble et forment des filaments qui vont se coller sur les parois des mitochondries. Ces organelles sont chargées de produire la plupart de l’énergie utilisée par la cellule, mais elles participent aussi à la défense cellulaire en causant de l’inflammation et la mort cellulaire. Dans ce cas sciencesetavenirprécis, les filaments de ZBP1 sont reconnus par une protéine antivirale sur la surface de la mitochondrie, nommée MAVS (pour « mitochondrial antiviral-signaling protein » en anglais). Cela active une deuxième vague d’interférons et active un processus inflammatoire qui finit par détruire la cellule.
« Les télomères, les mitochondries et l’inflammation sont trois marqueurs connus du vieillissement, mais ces trois éléments sont généralement étudiés séparément. Cependant, nos résultats montrent qu’ils travaillent en synergie, soulignant qu’il faut étudier leurs interactions afin de mieux comprendre le vieillissement et peut-être un jour pouvoir augmenter l’espérance de vie des humains », espère Gerald Shadel, spécialiste des mitochondries et le vieillissement à l’Institut Salk, et co-directeur de cette étude, dans un communiqué. Ces résultats rappellent aussi que le vieillissement cellulaire a une importante fonction anticancéreuse et que toute tentative pour repousser ce processus devra prendre en compte ce fait pour éviter qu’on vive plus longtemps, mais avec davantage de cancers.
sciencesetavenir