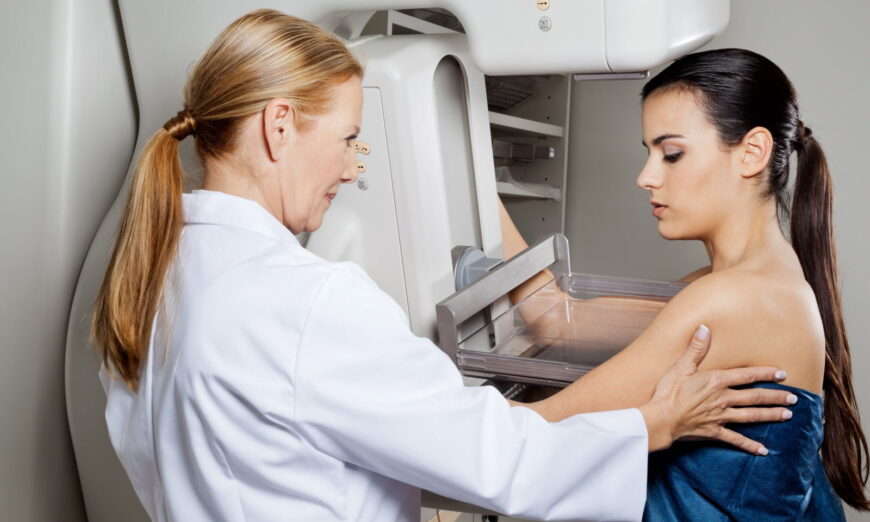
À l’heure actuelle, des techniques d’imagerie assez puissantes peuvent repérer des tumeurs et des métastases. Mais les cellules tumorales pourraient être détectées bien plus tôt et les laboratoires ont commencé à chercher des biomarqueurs circulants, afin d’améliorer la prise en charge des patients. Deux études récentes ont identifié des biomarqueurs d’intérêt.
Un biomarqueur est une caractéristique mesurable avec précision, utilisée comme indicateur d’une fonction du corps, d’une maladie ou de l’action d’un médicament. De ce fait, la recherche évolue sur l’identification des biomarqueurs et en particulier pour les cancers. C’est le cas par exemple de petits ou longs ARN non codants – il n’existe pas que des gènes codant pour des protéines dans notre génome – qui sont davantage exprimés dans certains cancers.
Les biomarqueurs sont très nombreux et donnent des indications biologiques différentes. Certains pourraient indiquer la présence d’un cancer, d’autres prévenir du risque de développer une métastase, et d’autres encore prédire la réponse au traitement des patients. Deux études ont visé à identifier des biomarqueurs spécifiques du cancer du sein, afin d’adapter le traitement des patientes le plus tôt possible.
LE CANCER DU SEIN EST LA TUMEUR MALIGNE LA PLUS FRÉQUENTE CHEZ LES FEMMES DANS LE MONDE.
Un biomarqueur dans la prévention du risque de développer un cancer secondaire
La première étude a identifié le miR-662, un microARN qui pourrait prédire à un stade très précoce la formation de métastases osseuses chez des patientes atteintes d’un cancer du sein, plus de 10 ans en amont. En effet, ce biomarqueur est associé aux métastases osseuses.
« Il joue un rôle dans la nidation des cellules cancéreuses au sein de la moelle osseuse pour former une micrométastase, avant le stade de la métastase qui pourra être détectée sur le plan clinique des années plus tard », explique à Futura le coauteur de l’étude Philippe Clézardin, directeur de recherche Inserm et professeur d’oncologie osseuse à l’université de Sheffield.
L’étude publiée dans le British Journal of cancer a notamment visé à quantifier les microARN circulant dans le sang des patientes dès le moment du diagnostic du cancer du sein ou juste après la chirurgie de tumeur et de les suivre pendant environ dix ans. « On peut prédire le risque de rechute métastatique à 5 ans avec le biomarqueur miR-662, mais il ne s’agit pas non plus d’un marqueur des métastases, précise le professeur.
On fait une corrélation entre la quantité au moment de l’acte chirurgical et la survenue au cours du temps de rechute. » Les métastases étant multifactorielles, le miR-662 n’est pas le seul facteur en jeu.
En tout, les chercheurs ont regardé l’expression de plus de 2 500 microARN différents avant de se focaliser sur le miR-662. Si le taux de ce dernier est élevé dans le sang d’une patiente, alors son risque relatif de développer une métastase osseuse est deux à trois fois plus élevé qu’une patiente avec un taux bas.
« Il existe un risque élevé que la patiente ait déjà des micrométastases dans la moelle osseuse. En effet, le prélèvement de sang est effectué après la chirurgie, donc l’analyse de sang ne peut pas provenir de la tumeur primitive et l’expression d’un facteur devient très intéressante. »
Si l’étude clinique est encore au stade expérimental, il faudra d’autres cohortes cliniques pour s’assurer que ce microARN est un biomarqueur valide « mais il en prend la bonne direction » selon le chercheur.
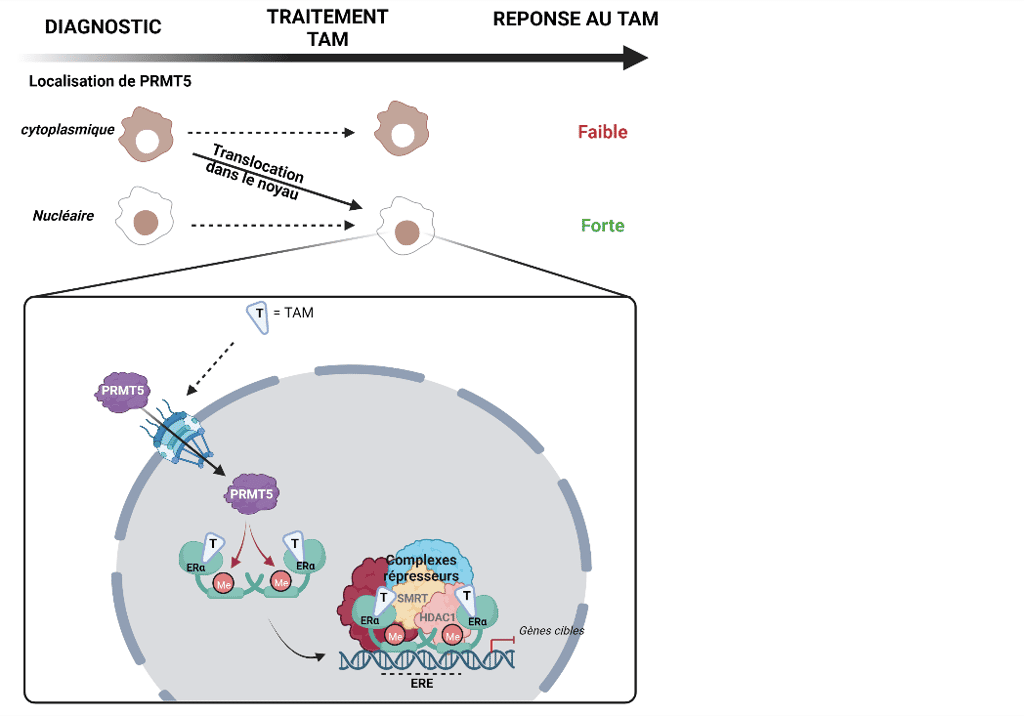
Publiée dans la revue EMBO Mol Med, la seconde étude a cette fois identifié une enzyme permettant de prédire la réponse des patientes atteintes d’un cancer du sein vis-à-vis du tamoxifène (Tam), un traitement anti-œstrogène de référence pour ces cancers. Un cancer du sein dit « luminal » peut bien être soigné avec le Tam, mais 25 % des patientes rechutent en raison d’une résistance au traitement. Or, il n’existe actuellement aucun biomarqueur prédictif de la sensibilité au Tam.
Toujours dans le but de trouver le meilleur traitement le plus tôt possible, l’étude a identifié le PMRT5 comme biomarqueur d’intérêt. Elle est co-dirigée par le Dr Muriel Le Romancer, directrice de recherche Inserm, et le Dr Olivier Trédan, oncologue au Centre de recherche en cancérologie de Lyon.
« Quand cette protéine est située dans le noyau des cellules, elle va participer à l’effet du Tam, qui est d’inhiber l’action du récepteur aux œstrogènes, explique Muriel Le Romancer. On propose de regarder au diagnostic l’expression de cette protéine avec un score.
Si le score est suffisamment élevé, cela signifie qu’elle est présente au bon endroit, dans le noyau, et on sait que la patiente va répondre au Tam. Alors que si on est au-dessous du score, la protéine est davantage dans le cytoplasme et la patiente aura peu de chances de répondre au traitement. »
On peut expliquer ce résultat par le fait que le récepteur aux œstrogènes se trouve dans le noyau. C’est un prérequis à l’action du Tam dans le noyau : il faut une certaine quantité de cette enzyme dans le noyau pour qu’un certain nombre de cellules tumorales soient régulées par le Tam.
À terme, « l’idée serait de combiner les traitements par anti-œstrogènes avec un médicament qui favorise la localisation de PRMT5 dans le noyau pour garantir une réponse au tamoxifène chez toutes les patientes préménopausées », conclut la chercheuse.
futura